Eficacia en alopecia de un acondicionador anticaída con Serenoa serrulata y tocoferol. Estudio piloto
Introducción
La alopecia androgenética (AGA), el tipo más común de pérdida de cabello, afecta a un elevado porcentaje de hombres con predisposición genética y a mujeres en edad menopáusica1,2. Se caracteriza por una miniaturización progresiva de los folículos pilosos en las áreas frontotemporal y del vértice craneal, consideradas regiones del cuero cabelludo sensibles a los andrógenos1,2.
La dihidrotestosterona (DHT), principal andrógeno derivado de la testosterona por acción de la 5 alfa reductasa, desempeña un papel cardinal en la patogenia de la AGA. La DHT, al actuar sobre los receptores de los andrógenos, provoca una miniaturización de los cabellos terminales y un acortamiento del ciclo anágeno3. Por otra parte, se ha demostrado la asociación entre el estrés oxidativo y la alopecia4.
La alopecia afecta negativamente a la autoestima y la calidad de vida de quienes la sufren2. Numerosos estudios han demostrado que la pérdida prematura del cabello provoca angustia y malestar emocional5, siendo el impacto mayor en las mujeres6. Además de suponer una gran carga anímica, la AGA precoz muestra una fuerte asociación con comorbilidades como la arteriopatía coronaria y el síndrome metabólico7. También se ha demostrado la relación de la AGA con casos graves de COVID‑19, denominada signo de Gabrin, en ambos sexos8,9.
La piel del cuero cabelludo presenta características diferenciales respecto a la de otras áreas corporales; contiene una elevada proporción de folículos pilosos, glándulas sebáceas y vasos sanguíneos10. En la alopecia existe cada vez más evidencia de que los andrógenos también pueden afectar, además de a los folículos pilosos, al tejido conjuntivo y las unidades pilosebáceas circundantes1.
El uso de sustancias de origen vegetal con potencial anticaída genera cada vez más interés como estrategia complementaria en la prevención de la alopecia. Estos compuestos, entre los que destacan el extracto de Serenoa serrulata y el tocoferol, se incluyen en productos como tónicos, promotores del crecimiento capilar, acondicionadores y champús11,12. Tanto S. serrulata, con propiedades inhibidoras de la 5 alfa reductasa13,14, como los tocotrienoles, potentes antioxidantes pertenecientes a la familia de la vitamina E, han demostrado un efecto beneficioso frente a la alopecia15‑17.
Con estos antecedentes, el objetivo principal de este estudio fue investigar si la aplicación de un acondicionador con extracto de S. serrulata y tocoferol reduce la caída del cabello tras 90 días de aplicación. Como objetivos secundarios, se estudiaron sus efectos en cuanto a seborregulación y firmeza del cuero cabelludo, su tolerabilidad y el grado de satisfacción de los pacientes con el producto.
Materiales y método
Estudio piloto unicéntrico, abierto, no aleatorizado, a simple ciego, de 90 días de duración, llevado a cabo en voluntarios que acudieron a la consulta dermatológica por pérdida generalizada de cabello. Se llevó a cabo entre marzo y julio de 2022.
El producto en estudio fue un acondicionador anticaída (C.N. 208832.0) que contenía zinc, tocoferol, extracto de S. serrulata y proteínas vegetales hidrolizadas, entre otros principios activos.
Tras una valoración clínica, los participantes utilizaron el acondicionador 3 o 4 veces por semana durante un periodo de 90 días. Se les pidió que se aplicaran el producto después del champú (tras aclarar el cabello con abundante agua), comenzando por las puntas del cabello y extendiéndolo después hacia las raíces. Tras realizar un ligero masaje, debían dejarlo reposar durante 3 minutos y enjuagarlo de forma abundante.
Los participantes no recibieron ningún otro producto anticaída por vía tópica ni oral durante el período de realización del estudio. Este se realizó en cumplimiento de las normas establecidas en la Guía para investigaciones con seres humanos y las directrices del Comité Científico de Seguridad del Consumidor18.
Criterios de inclusión y exclusión
Los participantes debían tener una edad comprendida entre los 18 y los 70 años, sufrir una pérdida generalizada de cabello, no presentar evidencia de padecer ninguna enfermedad sistémica, haber firmado el consentimiento informado específico y mostrar una motivación y disponibilidad suficientes.
Fueron criterios de exclusión que los participantes tuvieran patologías en el cuero cabelludo como psoriasis o dermatitis, que presentaran alergia o hipersensibilidad conocida a cualquiera de los componentes del producto en estudio, que estuvieran en periodo de embarazo o lactancia, o que hubieran utilizado cualquier producto cosmético, complemento nutricional o fármaco anticaída capilar en los 15 días previos al inicio del estudio.
Determinaciones clínicas
Se evaluó la pérdida de cabello mediante pruebas de lavado y de peinado realizadas por el personal técnico del estudio. En ellas se determinó el número de cabellos que se caían durante el lavado/peinado del cabello en condiciones estandarizadas. Los voluntarios acudieron a la visita sin haberse lavado el cabello al menos 48 horas antes y sin haberse peinado durante al menos las 24 horas previas, con el fin de evitar una reducción artificial en el porcentaje de cabellos en fase telógena.
Se valoró la firmeza del cuero cabelludo mediante indentometría (Indentometer® IDM 800 diámetro 1 mm, Courage & Khazaka, Köln, Alemania). Esta se basa en medir la deformación del cuero cabelludo inducida por las fuerzas de una sonda que desplazan la piel. Cuanto más firme/rígida es la piel del cuero cabelludo, menos profundo es el desplazamiento registrado. Una piel más firme/rígida significa un cuero cabelludo saludable con capacidad de presentar un buen anclaje del pelo.
El sebo del cuero cabelludo se valoró mediante sebometría (Sebumeter® SM 815, Courage & Khazaka, Köln, Alemania), con el fin de analizar las posibles propiedades seborreguladoras del producto en estudio. Los resultados se asignaron a una de las siguientes categorías: cuero cabelludo seco < 33 μg de sebo/cm²; normal 33‑66 μg de sebo/cm²; graso > 66 μg de sebo/cm².
El investigador principal completó un cuestionario de impresión clínica global para establecer la eficacia objetiva del producto en el punto temporal T90 o final de estudio. Asimismo, se utilizó una encuesta para valorar la eficacia y la tolerabilidad percibidas por los pacientes, además de su grado de satisfacción con las propiedades del producto. Los ítems fueron puntuados según una escala de acuerdo/desacuerdo de 5 grados.
Las pruebas técnicas y la valoración de la eficacia subjetiva y tolerabilidad del tratamiento se determinaron en el momento basal [T0], a los 45 [T45] y a los 90 días [T90].
Análisis estadístico
Se efectuó un análisis descriptivo de las variables, que se expresaron como media y desviación estándar o como porcentaje de variación. Se ajustaron modelos lineales de efectos mixtos (LMM) para evaluar la eficacia de cada tratamiento a lo largo del tiempo. El efecto del tratamiento sobre las medidas biométricas se interpretó comparando los valores correspondientes a cada punto temporal. En caso de distribución no normal de los datos, se realizó la prueba de rango con signo de Wilcoxon. Se estableció un valor de significación de 0,05 (intervalo de confianza del 95%).
Resultados
Completaron el estudio un total de 40 individuos. Un 60% de los participantes fueron mujeres y un 40% hombres. La edad media fue de 46 años (rango: 18‑65).
Pruebas de lavado y peinado
En las pruebas de lavado y peinado, la alopecia se redujo significativamente en un 38% y un 34% a los 45 y 90 días, respectivamente (Figura 1). Según la evaluación subjetiva de los pacientes, a los 45 días de aplicación del producto el 86,8% de ellos presentaron una mejoría en cuanto a alopecia (media del 34,9%). Esta se observó en el 81,1% de los sujetos a los 90 días de aplicación, con un promedio del 21,9%. Las diferencias fueron estadísticamente significativas.

Sebometría
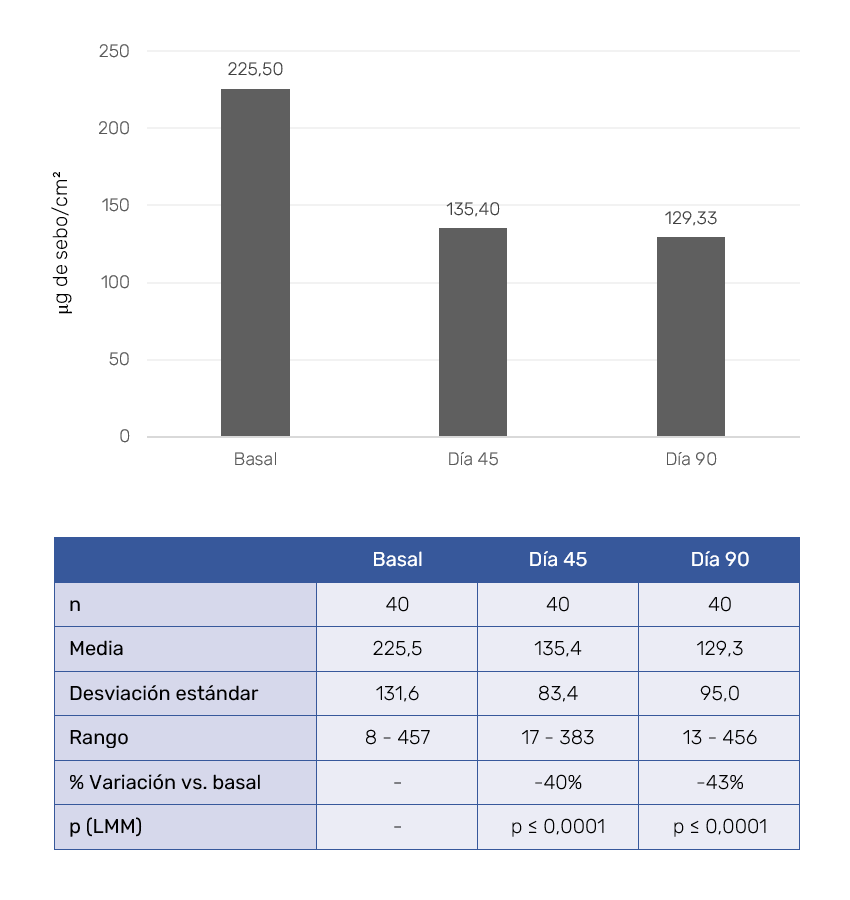
En cuanto a la regulación del sebo, se observó una reducción significativa del 40% y 43% a los 45 y 90 días, respectivamente (Figura 2). A los 45 días de aplicación del producto, el 85% de los pacientes reconocieron una mejoría en cuanto a reducción del sebo (media del 27,5%). Esta se observó en el 72,5% de los sujetos a los 90 días de aplicación del producto, con un promedio del 28,1%, siendo las diferencias estadísticamente significativas.
Indentometría
El desplazamiento de la sonda del indentómetro se redujo de forma significativa en un 21% y 19% a los 45 y 90 días del estudio, respectivamente, lo cual indicó que el cuero cabelludo adquirió mayor firmeza (Figura 3). Según la evaluación subjetiva de los pacientes, a los 45 días de aplicar el producto, el 75% de ellos mostraron una mayor firmeza del cuero cabelludo, con una mejoría media del 17,3%. Esta se observó en el 72,5% de los sujetos a los 90 días de aplicación del producto, con una media del 13,5%. Las diferencias fueron estadísticamente significativas.

Satisfacción con el tratamiento
Al finalizar el estudio, el 70% de los sujetos se mostraron satisfechos con el tratamiento. Un 60% opinaron que este había retrasado la caída del cabello, un 75% que se había reducido la irritación del cuero cabelludo, y sólo un 10% opinó que este seguía estando graso.
Tolerabilidad del tratamiento
Tras la aplicación del producto durante 90 días, no se detectaron ni se notificaron efectos secundarios significativos.
Discusión
Los resultados de este estudio sugieren la eficacia y tolerabilidad del acondicionador anticaída analizado, aplicado 3‑4 veces por semana durante un periodo de 90 días. La eficacia se ha demostrado en términos de reducción de la alopecia, disminución del sebo capilar y aumento de la firmeza del cuero cabelludo. En las pruebas de lavado y peinado, la alopecia se redujo significativamente en un 38% y un 34% a los 45 y 90 días, respectivamente.
El pelo protege el cuero cabelludo de factores ambientales como la radiación ultravioleta, los agentes químicos y los traumatismos19. El estrato córneo es una estructura multicapa que actúa como barrera y regula las funciones de la piel20,21. La alopecia reduce su capacidad de defensa y puede alterar su fisiología; varios estudios han demostrado que la AGA se asocia a una función de barrera alterada1. Las áreas sensibles a andrógenos muestran un agrandamiento significativo de las glándulas sebáceas, así como mayores niveles de DHT y 5 alfa reductasa en comparación con las zonas resistentes a andrógenos22,23.
El sebo secretado por el cuero cabelludo es una mezcla de triglicéridos, diglicéridos, ácidos grasos libres, escualenos, ésteres de colesterol, ésteres de cera y colesterol. Los cambios en su composición pueden influir en el desarrollo y progresión de la AGA24. En este estudio se observó una regulación significativa del sebo del cuero cabelludo, que se redujo en un 40% y 43% a los 45 y 90 días, respectivamente.
Chanpraphah et al evaluaron en 2021 las propiedades fisiológicas del cuero cabelludo mediante técnicas no invasivas, incluidos los valores de lípidos de la superficie cutánea (SSL), la pérdida de agua transepidérmica (TEWL) y la hidratación del estrato córneo (SCH), tanto en el vértice craneal como en las áreas occipitales. Los participantes fueron 31 sujetos con AGA de grado III‑VII y 31 controles sanos. En los pacientes con AGA, el cuero cabelludo del vértice craneal tuvo valores significativamente mayores de SSL (p = 0,03) y significativamente menores de SCH (p = 0,02) en comparación con la zona occipital. Respecto al grupo control, el grupo con AGA tuvo mayores cifras de SSL (p = 0,03) y una menor TEWL (p < 0,001) en el vértice craneal (ambas diferencias significativas), algo que no ocurrió en la zona occipital (no afecta de alopecia). Los niveles de SSL del grupo con AGA mostraron una correlación positiva con la gravedad de la alopecia (r = 0,61; p = 0,03)1.
En 2021, una revisión de la literatura concluyó que S. serrulata es efectivo para el tratamiento de la AGA con menos efectos secundarios que los presentados por finasterida o dutasterida25. También en el mismo año, un estudio clínico con el mismo principio activo, aunque unido a péptidos, y vehiculizado mediante microneedling, demostró eficacia en la disminución de la caída del cabello con aumento de grosor del tallo piloso26.
En nuestro estudio, tras aplicar el acondicionador durante 90 días, el cuero cabelludo de los pacientes adquirió mayor firmeza, con un desplazamiento significativamente menor de la sonda del indentómetro (un 21% y 19% a los 45 y 90 días, respectivamente), junto a una óptima seborregulación.
El acondicionador estudiado cuenta en su formulación con S. serrulata y tocoferol. Los polifenoles, flavonoides, terpenoides, carotenoides y ácidos grasos, componentes habituales en los extractos de plantas, contribuyen a la salud del folículo piloso27. Distintos ácidos grasos saturados de cadena media, junto con otros componentes bioactivos y fitoesteroles, podrían explicar los beneficios de S. serrulata en la inhibición de la 5 alfa reductasa y la reducción de la alopecia. Entre sus efectos se encuentran un aumento de la viabilidad celular, la estimulación del crecimiento del folículo piloso, una disminución de la respuesta inflamatoria, una reducción en modelos murinos de la expresión de TGF‑2 y de caspasa‑3 hidrolizada, así como una inhibición de la apoptosis13,16.
Uno de los factores que contribuyen a la AGA es la exposición al estrés oxidativo, con la formación de especies reactivas de oxígeno (ROS)4. Tal y como se demostró en un ensayo aleatorizado, la suplementación con cápsulas de tocotrienol aumentó significativamente el número de cabellos en 21 pacientes con alopecia respecto al grupo placebo (n = 17), lo cual se atribuyó a su actividad antioxidante, que ayudó a reducir la peroxidación lipídica y el estrés oxidativo en el cuero cabelludo17, datos que refrendan la acción antioxidante de la vitamina E.
Al finalizar el presente estudio, el 70% de los participantes se mostraron satisfechos con el acondicionador anticaída. Opinaron, entre otros aspectos, que este había retrasado la caída del cabello (60%), había reducido la irritación del cuero cabelludo (75%) y no había aumentado el grado de sebo (90%). En cuanto a la tolerabilidad, todos los participantes manifestaron la ausencia de efectos adversos asociados al producto.
Conclusiones
Los hallazgos de este estudio apuntan a un beneficio terapéutico, frente a la alopecia, de un acondicionador capilar con principios activos inhibidores de la 5 alfa reductasa (extracto de Serenoa serrulata), tocoferol, y zinc; aplicado de forma tópica 3‑4 veces/semana durante 90 días.
Esta eficacia se ha demostrado, tanto en mujeres como en hombres, en términos de reducción de la alopecia, disminución del sebo capilar y aumento de la firmeza del cuero cabelludo, con resultados significativos ya a los 45 días de aplicación. El producto fue bien tolerado y aceptado por los pacientes.
Dada la naturaleza piloto del estudio, se requieren investigaciones adicionales para confirmar estos beneficios en poblaciones más amplias de pacientes.
Conflicto de intereses
Javier Mira pertenece al organigrama industrial.
Bibliografía
- Chanprapaph K, Sutharaphan T, Suchonwanit P. Scalp Biophysical Characteristics in Males with Androgenetic Alopecia: A Comparative Study with Healthy Controls. Clin Interv Aging. 2021;16:781‑7. https://doi.org/10.2147/CIA.S310178
- Nestor MS, Ablon G, Gade A, Han H, Fischer DL. Treatment options for androgenetic alopecia: Efficacy, side effects, compliance, financial considerations, and ethics. J Cosmet Dermatol. 2021;20(12):3759‑81. https://doi.org/10.1111/jocd.14537
- Rojhirunsakool S, Suchonwanit P. Parietal scalp is another affected area in female pattern hair loss: an analysis of hair density and hair diameter. Clin Cosmet Investig Dermatol. 2018;11:7‑12. https://doi.org/10.2147/CCID.S153768
- Trüeb RM. Oxidative stress and its impact on skin, scalp and hair. Int J Cosmet Sci. 2021;43(Suppl 1):S9‑S13. https://doi.org/10.1111/ics.12736
- Kranz D. Young men’s coping with androgenetic alopecia: acceptance counts when hair gets thinner. Body Image. 2011;8(4):343‑8. https://doi.org/10.1016/j.bodyim.2011.06.006
- Davis DS, Callender VD. Review of quality of life studies in women with alopecia. Int J Womens Dermatol. 2018;4(1):18‑22. https://doi.org/10.1016/j.ijwd.2017.11.007
- Mysore V, Parthasaradhi A, Kharkar RD, Ghoshal AK, Ganjoo A, Ravichandran G et al. Expert consensus on the management of androgenetic alopecia in India. Int J Trichology. 2019;11(3):101‑6. https://doi.org/10.4103/ijt.ijt_24_19
- Wambier CG, Vaño-Galván S, McCoy J, Pai S, Dhurat R, Goren A. Androgenetic alopecia in COVID‑19: compared to age-matched epidemiologic studies and hospital outcomes with or without the Gabrin sign. J Am Acad Dermatol. 2020;83(6):e453‑e454. https://doi.org/10.1016/j.jaad.2020.07.099
- Lee J, Yousaf A, Fang W, Kolodney MS. Male balding is a major risk factor for severe COVID‑19. J Am Acad Dermatol. 2020;83(5):e353‑e354. https://doi.org/10.1016/j.jaad.2020.07.062
- Suchonwanit P, Triyangkulsri K, Ploydaeng M, Leerunyakul K. Assessing biophysical and physiological profiles of scalp seborrheic dermatitis in the Thai population. Biomed Res Int. 2019;2019:5128376. https://doi.org/10.1155/2019/5128376
- Jain PK, Das D, Singhai A. Alternative herbal drugs used for treating hair disease. Asian J Pharm Clin Res. 2016;9:75‑7.
- Park S, Lee J. Modulation of Hair Growth Promoting Effect by Natural Products. Pharmaceutics. 2021;13(12):2163. https://doi.org/10.3390/pharmaceutics13122163
- Penugonda K, Lindshield BL. Fatty Acid and Phytosterol Content of Commercial Saw Palmetto Supplements. Nutrients. 2013;5:3617‑33. https://doi.org/10.3390/nu5093617
- Pais P. Potency of a novel saw palmetto ethanol extract, SPET‑085, for inhibition of 5α-reductase II. Adv Ther. 2010;27:555‑63. https://doi.org/10.1007/s12325-010-0041‑6
- Murugusundram, S. Serenoa repens: Does it have any role in the management of androgenetic alopecia? J Cutan Aesthetic Surg. 2009;2:31. https://doi.org/10.4103/0974-2077.53097
- Zhu HL, Gao YH, Yang JQ, Li JB, Gao J. Serenoa repens extracts promote hair regeneration and repair of hair loss mouse models by activating TGF‑beta and mitochondrial signaling pathway. Eur Rev Med Pharm Sci. 2018; 22:4000‑8. https://doi.org/10.26355/eurrev_201806_15285
- Beoy LA, Woei WJ, Hay YK. Effects of tocotrienol supplementation on hair growth in human volunteers. Trop Life Sci Res. 2010;21(2):91‑9.
- European Commission. The SCCS´S Notes of Guidance for the Testing of Cosmetic Substances and their Safety Evaluation 9th Revision. 2016.
- Leerunyakul K, Suchonwanit P. Asian hair: a review of structures, properties, and distinctive disorders. Clin Cosmet Investig Dermatol. 2020;13:309‑18. https://doi.org/10.2147/CCID.S247390
- Wertz PW. Lipids and the permeability and antimicrobial barriers of the skin. J Lipids. 2018;2018:5954034. https://doi.org/10.1155/2018/5954034
- Suchonwanit P, Hector CE, Bin Saif GA, McMichael AJ. Factors affecting the severity of central centrifugal cicatricial alopecia. Int J Dermatol. 2016;55(6):e338‑343. https://doi.org/10.1111/ijd.13061
- Sawaya ME, Honig LS, Hsia SL. Increased androgen binding capacity in sebaceous glands in scalp of male-pattern baldness. J Invest Dermatol. 1989;92(1):91‑5. https://doi.org/10.1111/1523-1747.ep13071290
- Shamloul G, Khachemoune A. An updated review of the sebaceous gland and its role in health and diseases Part 2: Pathophysiological clinical disorders of sebaceous glands. Dermatol Ther. 2021;34(2):e14862. https://doi.org/10.1111/dth.14862
- Suzuki K, Inoue M, Cho O, Mizutani R, Shimizu Y, Nagahama T, Sugita T.Scalp Microbiome and Sebum Composition in Japanese Male Individuals with and without Androgenetic Alopecia. Microorganisms. 2021;9(10):2132. https://doi.org/10.3390/microorganisms9102132
- Martínez D, Simón L. Serenoa repens en el tratamiento de la alopecia androgenética. Revisión de la literatura. Medicina Estética. 2021;69(4):22‑27. https://doi.org/10.48158/MedicinaEstetica.069.03
- Lorente E, León F, Pérez ML. Tratamiento de alopecia androgenética con Sabal serrulata y péptidos biomiméticos vehiculizados con microneedling. Medicina Estética. 2021;68(3):27‑33. https://doi.org/10.48158/MedicinaEstetica.068.02
- Działo M, Mierziak J, Korzun U, Preisner M, Szopa J, Kulma A. The potential of plant phenolics in prevention and therapy of skin disorders. Int Mol Sci. 2016;17:160. https://doi.org/10.3390/ijms17020160




