Tratamiento con tecnología de plasma fraccional para arrugas y laxitud
de los párpados superiores
for wrinkles and laxity of the upper eyelids
Introducción
La piel de los párpados es una de las que primero sufren los efectos de la exposición a la luz solar, acelerando su envejecimiento, que se manifestará como laxitud, desarrollo de arrugas, y en un grado más severo, ptosis o dermatocalasia. El grado de afectación del área palpebral determinará el tratamiento de elección. Las posibilidades son múltiples, desde la cirugía convencional hasta el empleo de láseres, bien en modo ablativo o no ablativo1,2.
La blefaroplastia sigue siendo la opción quirúrgica por excelencia cuando la laxitud cutánea y la ptosis palpebral son acusadas. Normalmente se obtienen buenos resultados y menos complicaciones en el tratamiento del párpado superior que en el inferior3,4. Una alternativa a la blefaroplastia convencional es realizar la cirugía asistida con láser CO₂; lo que reduce el tiempo intraoperatorio, controla el sangrado, disminuye el edema y el tiempo de recuperación del paciente y tiene menor tasa de complicaciones5. No obstante, muchos pacientes no desean pasar por el quirófano, teniendo en cuenta la anestesia general, el tiempo de recuperación y las complicaciones inherentes a la técnica.
La búsqueda de alternativas menos invasivas, encaminadas a paliar los inconvenientes citados, propició el empleo de láseres fraccionales6,7, tanto de CO₂ como de Er:YAG para lograr un tensado eficaz de la piel de los párpados sin las complicaciones propias de los láseres ablativos inicialmente empleados8.
Desde hace varios años se dispone de un nuevo procedimiento que utiliza la energía del plasma, liberada en forma de pulsos, para producir un efecto térmico sobre la piel9. El plasma no depende de cromóforos diana y produce una vaporización escasa sobre el tejido9,10. En medicina tienen interés los denominados plasmas no térmicos o fríos, cuya ionización se logra a baja presión. Los plasmas fríos de presión atmosférica son de particular interés porque pueden interactuar con tejidos vivos, utilizando sus propiedades en aplicaciones biomédicas, incluyendo esterilización, preparación de polímeros, cicatrización de heridas, eliminación de tejidos o células, tratamiento dental y cosmético y terapia de cáncer10‑12. La aparición, en la última década del siglo XX de los microplasmas, ha propulsado nuevas investigaciones12,13.
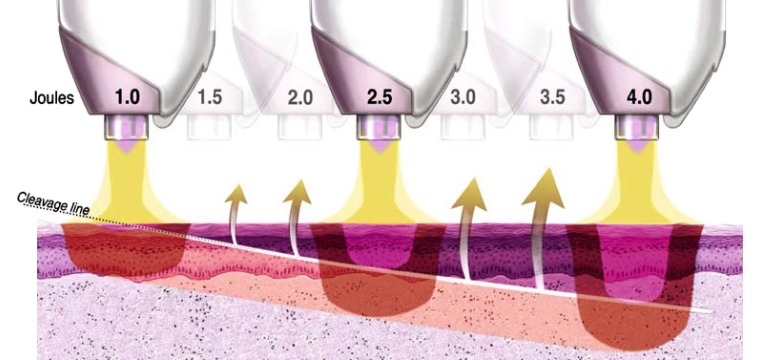
En relación al tratamiento de la dermatocalasia y la ptosis palpebral, el plasma se emite en pulsos de energía de milisegundos que afecta a la epidermis cuando se trabaja con 1 o 2 julios, pero si se aumenta la energía a 3 o 4 julios se alcanza la dermis papilar, lo que indica que la profundidad del efecto depende de la cantidad de energía entregada por pulso14. La energía de plasma produce primero una zona de daño térmico (ZDT), induciendo vacuolización celular, lo que limita la absorción de más energía. En torno a ella, surge una zona de modificación térmica (ZMT) con células térmicamente estimuladas, aunque viables, que desarrollará una intensa actividad fibroblástica (Figura 1). Unos 10 días después del tratamiento hay formación de fibras de colágeno y elastina. Ambas zonas (ZDT y ZMT) dependerán de la energía utilizada en cada paciente15,16. El tratamiento deja una capa de epidermis desecada intacta que se desprende de 96 horas después, en función de la energía aplicada, y actúa a modo de apósito biológico para una recuperación más rápida9,15,17.
El objetivo de este estudio es valorar la eficacia del tratamiento con energía de plasma en la mejora estética y funcional de los parpados superiores, teniendo en cuenta los efectos secundarios, la tolerancia y la satisfacción del paciente.
Material y método
Se realizó un estudio prospectivo y longitudinal con 12 pacientes, de edades comprendidas entre 45 y 72 años (55,67 ± 8,92) con tipo de piel II a IV de la clasificación de Fitzpatrick, mediante el dispositivo Plasmage® (Brera Medical Tecnologies srl, Ogliastro Cilento, Italia) en forma ambulatoria, en nuestra clínica.
El tratamiento se realiza acercando la punta de la pieza de mano, sin tocar la piel del párpado. En cada pulso la diferencia de potencial que existe entre la punta y la piel proyecta la energía de plasma, produciendo la contracción del tejido a través de la vaporización de los corneocitos afectados, y su posterior micro-cicatrización. Se actuó aplicando pulsos de energía de plasma fraccional en las zonas con laxitud de tejido siguiendo el eje longitudinal del párpado superior, con separación de 1 mm entre pulsos; tratando aproximadamente un tercio de la superficie total del parpado superior, aplicando 2 W de potencia, con ajuste fraccional 3, y densidad de energía por disparo de 6 mJ/mm².
Los criterios de inclusión fueron: pacientes con exceso de piel y/o algún grado de ptosis palpebral, que no deseaban realizarse una intervención quirúrgica ni tratamientos ablativos con láser de CO₂, comprometidos a contactar con la clínica si se presentaba cualquier incidencia y a realizarse una fotografía antes y al mes de finalizado el procedimiento.
Fueron excluidos pacientes que se hubieran realizado tratamientos estéticos en la zona periorbitaria en los últimos 12 meses, tales que toxina botulínica, rellenos o peeling. Tampoco los que se hubieran tratado con láser y/o blefaroplastia previa. No se admitieron embarazadas o mujeres en periodo de lactancia, ni pacientes con infección alrededor de los ojos, cicatrices patológicas (queloides o cicatrices hipertróficas), portadores de enfermedades autoinmunes, o que hubieran estado en tratamiento con isotretinoína en los últimos 6 meses.
Todos los participantes firmaron un consentimiento informado específico. Se tomaron fotografías en proyección frontal con los ojos abiertos, antes y un mes después del tratamiento, con una cámara digital Canon EOS 600D, objetivo Macro Lens 100 mm y flash Macro Ring Lite (Canon, Tokyo, Japan).
Tras una limpieza de la zona se aplicó, durante 45 minutos, crema anestésica en formulación magistral (tetracaína 6%, lidocaína 7% y prilocaína 7%; Farmacia Cayetano, Alicante, España). Para mantener el confort del paciente, solo se retiró la crema anestésica del ojo a tratar, y posteriormente se hizo lo mismo con el otro. Se marcó el parpado y se desinfectó con clorhexidina 2% previamente al tratamiento. Al terminar la técnica, se cubrió la zona con gasas húmedas frías, durante 15 minutos, y se aplicó una pomada con corticoide (Diproderm, Merck, Sharp & Dohm, Madrid, España). Se instruyó a los pacientes por escrito para que se aplicaran una gota de Tobradex® (Novartis, Barcelona, España) cada 12 h durante 3 días. Hasta la caída de las costras (entre 5 y 10 días) debían limpiarse las zonas tratadas con antiséptico y gasas estériles, dos veces al día, y no usar maquillaje. Además, debían evitar la exposición solar ayudándose de gafas y/o sombrero. Tras caer las costras se recomendó aplicar una crema regenerante, Cicaplast (L’Oreal, París Francia) y protección solar, Heliocare SPF 50® (Cantabria, Santander, España) durante 3 meses.
Se registraron los posibles efectos adversos que pudiesen aparecer hasta 2 meses después del tratamiento, referentes a edema, eritema, hipopigmentación, hiperpigmentación e infección. Se consideraron leves, si se resolvían en menos de 3 días; moderados, entre 4 y 30 días, y graves si persistían más de 30 días.
Para la valoración de resultados se utilizó la Escala de Laxitud Facial, que se valida exclusivamente mediante fotografías con los ojos abiertos. Se valoró el grado de laxitud en el párpado superior teniendo en cuenta la separación del pliegue palpebral del borde de implantación de las pestañas18. La escala se compone de 10 clases, o bocetos, que permiten comparar las muestras a fin de catalogarlas (Figura 2). La clase 0 representa ausencia de laxitud y el resto, de 1 a 9 un grado progresivo de laxitud. Sin embargo, con fines prácticos, clínicos y estadísticos, estas 9 clases se redujeron a 3 niveles de laxitud: leve, moderado y severo.

La tolerancia al dolor se evaluó mediante una Escala Visual Analógica (EVA) de 100 mm de longitud sobre papel, siendo 0 dolor nulo, y 100 dolor extremo. También se realizó una valoración del grado de satisfacción del paciente un mes después de finalizado el tratamiento.
Las variables cuantitativas se han descrito mediante la media aritmética y la desviación típica (DT) y las variables categóricas a través de porcentajes. Las diferencias entre las puntuaciones de la escala de laxitud antes (F0) y al mes de tratamiento (F1) se evaluaron mediante el test de rangos con signo de Wilcoxon, ya que el tamaño de muestra es pequeño (n=24 párpados superiores en 12 pacientes), y con una variable que no sigue una distribución normal. Todos los test aplicados lo fueron a dos colas y se consideraron estadísticamente significativas todas las p < 0,05.
Resultados
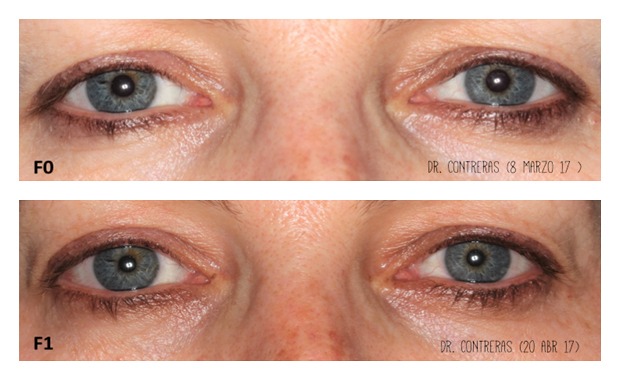
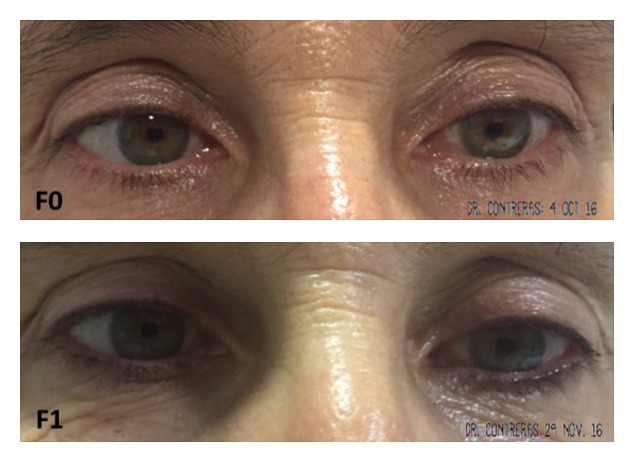
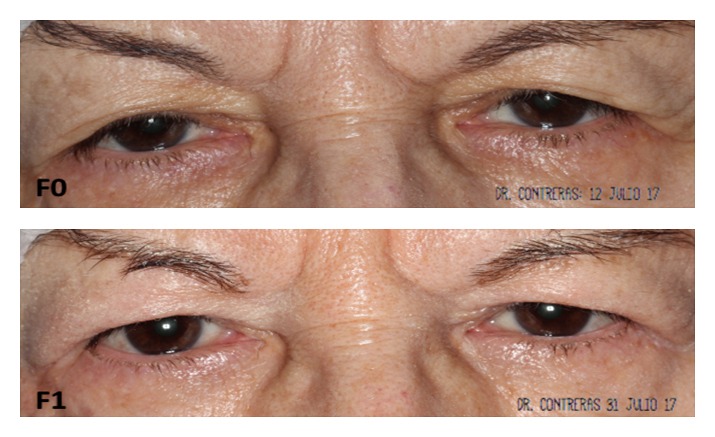
Todos los pacientes acudieron a las visitas programadas y a las sesiones de tomas de imágenes sin que hubiera ningún abandono. La puntuación media en la escala de laxitud en el ojo derecho fue de 5,43 ± 1,24, antes, y 3,83 ± 1,47 después del tratamiento. La diferencia fue estadísticamente significativa (p < 0,002). Con respecto al ojo izquierdo las puntuaciones medias, antes y después del tratamiento, fueron de 5,42 ± 1,24 y 4,00 ± 1,41, respectivamente, con diferencia estadísticamente significativa (p < 0,002). Si se considera la muestra de ambos ojos (n=24) la puntuación media en la escala de laxitud, antes y después del tratamiento, fue de 5,42 ± 1,21 y 3,92 ± 1,41, respectivamente; esta diferencia fue estadísticamente significativa (p < 0,001). Cabe comentar que los pacientes 8 y 9, de 69 y 72 años respectivamente, obtuvieron una mejoría muy leve, y al paciente 7 no se le apreció mejoría en el ojo derecho. En término de clases hubo una mejoría en el 96% de las muestras, lo cual supuso, en particular, mejorar 3 clases en 5 muestras, 2 clases en 3 muestras, y 1 clase en 15 muestras (Figuras 3–6).


Se revisaron los pacientes al mes y a los 2 meses para recoger los datos de posibles efectos adversos producidos por la técnica. Todos los pacientes presentaron edema en el parpado superior después de la prueba, nueve de los cuales se resolvieron en 1 día (leve), y tres en 5‑6 días (moderado). Ninguno fue etiquetado de grave. La piel eritematosa después de la prueba se apreció en todos pacientes, y en ocho de ellos se mantuvo 3 días (leve), y en cuatro duró hasta 7 días (moderado). Solo hubo un paciente con hiperpigmentación moderada que revertió antes del mes. No se apreció ningún episodio de hipopigmentación, ni de infección.
El tratamiento fue bien tolerado en general, con una puntuación promedio de dolor de 36,75 ± 14,16 sobre una escala de 1 a 100. El 80% presentaron dolor leve (media de 28,5 ± 7,11), mientras que en el 20% restante refirieron dolor moderado (53,25 ± 8,54).
Respecto al grado de satisfacción alcanzado por los pacientes, el 100% de los pacientes respondieron que el tratamiento les había sido útil; el 67% había notado una mejoría estética y en igual porcentaje se repetirían la prueba si fuese necesario. Finalmente, un 75% notaron los párpados menos pesados, incluyendo las dos pacientes con mayor afectación, una de ellas catalogada como severa en la escala de laxitud (Figura 7).
Discusión
Existe una demanda real de tratamientos para el rejuvenecimiento periorbitario, ya que los parpados debido a su configuración anatómica sufren precozmente los efectos del envejecimiento1,6. Las técnicas invasivas, como la blefaroplastia asistida o no con láser de CO₂, son adecuadas para el tratamiento de ptosis severas acompañadas de laxitud importante de la piel, aunque es una técnica asociada a complicaciones, algunas graves3‑5.
Una alternativa no desdeñable es el empleo de láser de CO₂ fraccional6,7. No obstante, para esta práctica debe realizarse un largo aprendizaje, unido a la correcta selección de los parámetros de aplicación láser, conociendo bien el grosor de la piel en las distintas partes de ambos párpados, así como la relación con el esqueleto conectivo y los ligamentos de retención5,7,8. Cabe añadir que su eficacia va ligada íntimamente a la cantidad de depósito térmico que se puede efectuar en esta particular área, pues a medida que se deposita más energía aumentan las posibles complicaciones, siendo habituales el edema y el eritema (que puede prolongarse hasta 3 semanas)8. Además, se han descrito complicaciones graves, casi siempre asociadas a una mala aplicación de la técnica, tales que ectropión, infecciones o quemaduras corneales8,9,12.
El tratamiento con energía plasma puede ser una alternativa prometedora para mejorar las arrugas de la piel de los párpados, con menos efectos secundarios que los que muestra la blefaroplastia tradicional o los tratamientos láser9,16,17,19. De hecho, los efectos secundarios asociados al estudio que se presenta fueron eritema y edema, y un caso de hiperpigmentación que se resolvió antes del mes. Sin embargo, hay que ser prudentes ya que el tiempo máximo de revisión fueron solo 2 meses, aunque en la literatura no se han informado discromías permanentes en seguimientos de 6 a 12 meses17.
La energía plasmática no es ablativa, y en contraste con el láser, su uso deja una capa de epidermis desecada intacta que actúa como apósito biológico natural, que se desprende hacia los 4‑5 días y promueve una recuperación más rápida9,14,15, permitiendo al paciente una reincorporación anticipada a su vida habitual. La técnica es una alternativa viable, de fácil ejecución, que se tolera de modo aceptable y no requiere pauta de antibioterapia preventiva ni posoperatoria.
Se han encontrado en la literatura algunos estudios con tecnología plasma que presentan similares resultados15,17,19,20. La tolerancia al dolor también es un criterio importante al aplicar cualquier técnica. Cuando se emplea láser fraccional puede ser suficiente aplicar anestesia tópica en crema, aunque algunos autores son partidarios de emplear bloqueos nerviosos y sedantes suaves7,21. En este estudio solo se aplicó anestesia tópica, y los pacientes toleraron bien el tratamiento: el 80% etiquetaron el dolor como leve, y el 20% lo refirió como moderado.
Respecto de la eficacia del tratamiento, un 21% de los pacientes mejoraron en 3 clases, 12% en 2 clases, y el 63 % en una clase. Estos porcentajes podrían ser mejores si se efectuaran 2 o 3 sesiones adicionales; como muestran los buenos resultados de algunos estudios16,20. Una segunda sesión podría alcanzar un resultado más satisfactorio en los pacientes evaluados como categoría severa, que suelen ser los que tienen más edad. Sin embargo, se debe reseñar que este estudio presenta una muestra de tamaño limitado, y con edades no uniformes, lo que aconseja que se realicen estudios en un mayor grupo de población. Además, sería interesante contrastar los resultados alcanzados por medio de la tecnología plasma con aquellos que se obtienen con láser fraccional.
Conclusiones
La eficacia de la energía de plasma a baja presión y temperatura es una alternativa para el tratamiento de la laxitud de la piel palpebral, especialmente para los pacientes que deseen mejorar el aspecto de los párpados superiores sin someterse a blefaroplastia o láser CO₂ fraccional. Es una técnica ambulatoria, bien tolerada, con escasos efectos secundarios, pronta recuperación y relación coste-beneficio asumible.
No obstante, se necesitan estudios aleatorizados, doble ciego y bien diseñados para establecer objetivamente las indicaciones en pacientes con ptosis palpebral moderada y severa, a fin de conocer bien los límites de esta técnica.
Declaración
El autor manifiesta no tener conflicto alguno de intereses con lo publicado y agradece la contribución del Dr. Justo M. Alcolea a la redacción final del artículo.
Bibliografía
- Fathi R, Pfeiffer ML, Tsoukas M. Minimally invasive eyelid care in dermatology: medical, laser, and cosmetic therapies. Clin Dermatol. 2015; 33(2):207‑216. https://doi.org/10.1016/j.clindermatol.2014.10.012
- Brauer JA, Patel U, Hale EK. Laser skin resurfacing, chemical peels, and other cutaneous treatments of the brow and upper lid. Clin Plast Surg. 2013; 40(1):91‑99. https://doi.org/10.1016/j.cps.2012.08.006
- Lelli GJ Jr, Lisman RD. Blepharoplasty complications. Plast Reconstr Surg. 2010; 125(3):1007‑1017. https://doi.org/10.1097/prs.0b013e3181ce17e8
- Mack WP. Blepharoplasty complications. Facial Plast Surg. 2012; 28(3):273‑287. https://doi.org/10.1055/s-0032-1312705
- Leclère FM, Alcolea J, Mordon S, et al. Long‑term outcomes of laser assisted blepharoplasty for ptosis: about 104 procedures in 52 patients. J Cosmet Laser Ther. 2013; 15(4):193‑199. https://doi.org/10.3109/14764172.2012.758385
- Alexiades-Armenakas MR, Dover JS, Arndt KA. The spectrum of laser skin resurfacing: nonablative, fractional, and ablative laser resurfacing. J Am Acad Dermatol. 2008; 58(5):719‑740. https://doi.org/10.1016/j.jaad.2008.01.003
- Bae-Harboe YS, Geronemus RG. Eyelid tightening by CO2 fractional laser, alternative to blepharoplasty. Dermatol Surg. 2014; 40 Suppl 12:S137‑S141. https://doi.org/10.1097/dss.0000000000000165
- Ramsdell WM. Fractional CO2 Laser Resurfacing Complications. Semin Plast Surg. 2012; 26(3):137‑140. https://doi.org/10.1055/s-0032-1329415
- Foster KW, Moy RL, Fincher EF. Advances in plasma skin regeneration. J Cosmet Dermatol. 2008; 7(3):169‑179. https://doi.org/10.1111/j.1473-2165.2008.00385.x
- Laroussi M, Lu X, Keidar M. Perspective: The physics, diagnostics, and applications of atmospheric pressure low temperature plasma sources used in plasma medicine. Journal of Applied Physics. 2017; 122(2):1‑19‑020901. https://doi.org/10.1063/1.4993710
- Heinlin J, Morfill G, Landthaler M, et al. Plasma medicine: possible applications in dermatology. J Dtsch Dermatol Ges. 2010; 8(12):968‑976. https://doi.org/10.1111/j.1610-0387.2010.07495.x
- Morfill GE, Kong MG, Zimmermann JL. Focus on Plasma Medicine. New J. Phy. 2009;11‑115011. https://doi.org/10.1088/1367-2630/11/11/115011
- Loesch MM, Somani AK, Kingsley MM, Travers JB, Spandau DF. Skin resurfacing procedures: new and emerging options. Clin Cosmet Investig Dermatol. 2014; 7:231‑241. https://doi.org/10.2147/ccid.s50367
- Bogle MA, Arndt KA, Dover JS. Evaluation of plasma skin regeneration technology in low‑energy full‑facial rejuvenation. Arch Dermatol. 2007; 143(2):168‑174. https://doi.org/10.1001/archderm.143.2.168
- Kilmer S, Semchyshyn N, Shah G, Fitzpatrick R. A pilot study on the use of a plasma skin regeneration device (Portrait PSR3) in full facial rejuvenation procedures. Lasers Med Sci. 2007; 22(2):101‑109. https://doi.org/10.1007/s10103-006-0431-9
- Rossi E, Farnetani F, Trakatelli M, Ciardo S, Pellacani G. Clinical and Confocal Microscopy Study of Plasma Exeresis for Nonsurgical Blepharoplasty of the Upper Eyelid: A Pilot Study. Dermatol Surg. 2018; 44(2):283‑290. https://doi.org/10.1097/dss.0000000000001267
- Giroux PA, Hersant B, SidAhmed-Mezi M, Pizza C, La Padula S, Meningaud JP. The Outcomes Assessment of the Plasma Blade Technology in Upper Blepharoplasties: A Prospective Study on a Series of 25 Patients. Aesthetic Plast Surg. 2019; 43(4):948‑955. https://doi.org/10.1007/s00266-019-01360-2
- Leal Silva HG. Facial Laxity Rating Scale Validation Study. Dermatol Surg. 2016;42(12):1370‑1379. https://doi.org/10.1097/dss.0000000000000915
- Cantisani C, Amori P, Vitiello G, et al. Nonsurgical blepharoplasty. Dermatol Ther. 2019; 32(6):e13119. https://doi.org/10.1111/dth.13119
- Baroni A. Non-surgical blepharoplasty with the novel plasma radiofrequency ablation technology. Skin Res Technol. 2020; 26(1):121‑124. https://doi.org/10.1111/srt.12774
- Yates B, Que SK, D'Souza L, Suchecki J, Finch JJ. Laser treatment of periocular skin conditions. Clin Dermatol. 2015; 33(2): 197‑206. https://doi.org/10.1016/j.clindermatol.2014.10.011
- Toyos MM. Continuous Wave Fractional CO2Laser for the Treatment of Upper Eyelid Dermatochalasis and Periorbital Rejuvenation. Photomed Laser Surg. 2017; 35(5):278‑281. https://doi.org/10.1089/pho.2016.4225

