Actualización en el tratamiento del melasma. Revisión sistemática
Introducción
El melasma se define como un trastorno de la pigmentación cutánea producido por una alteración en la melanogénesis. La etiopatogenia multifactorial y las distintas alternativas de tratamiento dificultan un abordaje óptimo, conduciendo a errores terapéuticos. Es aconsejable definir algoritmos terapéuticos para lograr una pronta mejoría y optimizar los recursos económicos. El melasma es una enfermedad adquirida relativamente común, caracterizada por un patrón de hiperpigmentación facial crónica y simétrica, con facilidad para la recidiva. Suele afectar las áreas más expuestas al sol: mejillas, frente, labio superior, nariz y mentón. Según su distribución facial, se clasifica en tres tipos: centrofacial, malar y mandibular.
Se diagnostica clínicamente, siendo útiles para el diagnóstico el examen con lámpara de Wood y la dermatoscopia. La prevalencia varía de 1,5 a 33,3% dependiendo de la etnia, género, tipo de piel y ubicaciones geográficas1. El melasma, como la hiperpigmentación postinflamatoria, es más frecuente en pacientes con fototipos oscuros2,3. Suele tener una mayor afectación en la raza asiática, hispánica y africana que en la caucásica; en varones de raza caucásica afecta al 10% y en raza hispánica al 14,5%4. Es habitual que se manifieste sobre la tercera o cuarta década de la vida; con inicio más temprano en fototipos de piel clara1. Destaca también la asociación entre la exposición de calor ocupacional y la severidad del melasma4.
El melasma tiene mayor prevalencia en mujeres que reciben anticonceptivos y durante el embarazo (segundo y tercer trimestre), donde aumentan los niveles de hormonas placentarias, ováricas y pituitarias, las cuales son un estímulo para la melanogénesis1. Sarkar et al evidenciaron en su estudio que un 15,2% de las pacientes con melasma eran gestantes4. No obstante, un aumento de los niveles séricos de testosterona y la aromatización de testosterona a estradiol podrían inducir la hiperpigmentación en el melasma1. Histológicamente se caracteriza por un depósito excesivo de melanina en la epidermis (melasma epidérmico: 70%), en la dermis (melasma dérmico: 10%) o ambos (tipo mixto: 20%). Pueden observarse melanocitos grandes y melanosomas aumentados en la epidermis con gran cantidad de producción de melanina e incremento de la migración de pigmento a través de las capas dermo-epidérmicas5. En el subtipo dérmico se pueden observar melanófagos e infiltrados linfohistiocíticos con depósitos de melanina. El melasma mixto tiene las características combinadas de los tipos epidérmico y dérmico.
Los cambios histopatológicos del melasma se superponen al fotoenvejecimiento5,6. La dermis de la piel del melasma puede presentar elastosis solar en grado variable (83% al 93%) y alteración de la membrana basal, lo que favorece el paso de melanina y melanocitos a la dermis. Además, la exposición crónica a los RUV eleva los niveles de metaloproteinasas, MMP‑2 y MMP‑9, que degradan el colágeno tipo IV y VI5,6; el aumento de vascularización obedece al incremento del factor de crecimiento vascular endotelial (VEGF), el factor de células madre (SCF) y la óxido nítrico sintetasa inducible (iNOs)7,8. En la dermis suele observarse un aumento de fibroblastos; lo que también favorece la secreción de SCF que, a su vez, estimula la vía de la tirosin kinasa6. Al mismo tiempo, los mastocitos incrementan la liberación de histamina que estimula la melanogénesis. También, se ha planteado la hipótesis de que los sebocitos contribuyan al desarrollo del melasma al secretar citocinas y factores de crecimiento, como IL‑1‑α, IL‑6 y angiopoyetina9. Por último, el mayor número de receptores de estrógenos y progesterona en la dermis pueden activar las vías de la tirosinasa y el MITF (Melanocyte Inducing Transcription Factor, factor de transcripción inductor de melanocitos)6.
De los medicamentos empleados, la hidroquinona (HQ), un inhibidor de la tirosinasa, se considera el gold standard a pesar de sus reacciones adversas locales (hipersensibilidad, oscurecimiento o irritación transitoria de la piel). Es eficaz sola o en combinación con otros agentes10, como el ácido azelaico (AA), que incrementa la absorción a través de la piel de ambos compuestos, además de inhibir per se la tirosinasa11. El AA 20% presenta actividad antiinflamatoria y podría actuar previniendo la hiperpigmentación postinflamatoria y el melasma, siendo su eficacia aproximadamente la misma que la de la HQ 4%, con menos efectos adversos11,12. El ácido kójico, 5‑hidroxi-2‑hidroximetil-4‑pirona, se suele utilizar en concentraciones de 2% a 4%. Es seguro, efectivo y reduce la pigmentación de la piel sin efectos secundarios13.
El ácido ascórbico (vitamina C) disminuye la oxidación de la dopaquinona, la actividad de la tirosinasa, reduce el daño dérmico, promueve la síntesis de colágeno y tiene efectos antioxidantes y fotoprotectores; además, es capaz de interactuar con el cobre al reducir la síntesis de dopaquinona a DOPA. A todo ello se suma su efecto fotoprotector de los rayos UVA y UVB, evitando la producción de radicales libres7.
Los corticoides tópicos (CT) se utilizan combinados con otros activos por su capacidad para disminuir la irritación de la piel. Sin embargo, pueden provocar efectos adversos como telangiectasias, dermatitis acneiforme, atrofia e hipertricosis. Los retinoides ejercen su acción despigmentante a través de una doble vía: aumentando el recambio de queratinocitos y reduciendo la transferencia de melanosomas de los melanocitos a los queratinocitos. El ácido tranexámico (AT), o 4‑aminometil-nafténico, actúa bloqueando reversiblemente la unión del plasminógeno a la plasmina en los queratinocitos, además de competir con la tirosina inhibiendo la transformación de tirosina en DOPA. Por otra parte, el AT inhibe la prostaglandina E2 (PG E2), que tiene un papel importante en las vías de señalización del crecimiento, diferenciación y apoptosis de los melanocitos; así como la estimulación de la formación de dendritas en los melanocitos y la activación de la tirosinasa14. El AT también disminuye los niveles de VEGF y entotelina‑1, reduciendo la vascularización en las lesiones de melasma15.
Los peelings químicos, utilizados en combinación con agentes tópicos, suelen ser más efectivos en el melasma epidérmico. Se emplean habitualmente alfa-hidroxiácidos (láctico y glicólico), salicílico y TCA. A lo anterior se ha sumado el empleo de láseres para tratar las lesiones pigmentarias epidérmicas y dérmicas benignas en los últimos 20 años.
El láser de Nd:YAG de 1064 nm es capaz de tratar lesiones dérmicas por su penetración más profunda y escasa absorción en la epidermis. No obstante, su eficacia presenta una alta tasa de recurrencia, por lo que se están empleando láseres de Nd:YAG en modo Q‑Switched con baja fluencia (0.8‑2 J/cm²), spots grandes (6‑8 mm), frecuencias altas (10 Hz) y múltiples pases3,4. Se pretende que la fototermólisis subcelular disminuya la incidencia de complicaciones y una recuperación más rápida de la piel tratada. Como el anterior, los láseres que emiten en picosegundos poseen mayor efecto fotomecánico, fragmentando más el pigmento para minimizar el daño colateral1. Sobre el beneficio de los láseres ablativos en el melasma, se especula si obedece a su capacidad de lograr una ablación y coagulación dérmica profunda, lo que favorecería la penetración de fármacos al eliminar el estrato córneo y las capas más superficiales rompiendo la barrera cutánea16.
El PRP se emplea por su potencial capacidad reparadora, aunque su aplicación en el melasma no está bien contrastada. Solo hay coincidencia en señalar las bajas probabilidades de presentar reacciones adversas por su origen autólogo; aunque es una opción segura no indica que sea eficaz.
En lo que hay acuerdo es en emplear una fotoprotección de amplio espectro (UVA, UVB, luz visible e infrarrojo cercano) por la sinergia protectora ante la exposición de las diferentes longitudes de onda17. Es necesario destacar que el dióxido de titanio y el óxido de zinc son los fotoprotectores más eficaces contra la luz visible18. En pacientes embarazadas, el protector solar puede ser la única opción terapéutica disponible, por lo que cabe educarlas sobre los efectos de la exposición solar y los beneficios de la fotoprotección de amplio espectro.
El objetivo del presente estudio es evaluar la eficacia de los diferentes tratamientos propuestos para el melasma.
Material y método
Se ha realizado una revisión sistemática de artículos completos, en inglés, de enero de 2019 a junio de 2020, basados en ensayos clínicos originales sobre pacientes de ambos sexos mayores de 18 años, en las bases de datos PubMed (Medline) y Cercabib (Universidad de Barcelona). Se revisaron los ensayos clínicos de enero de 2016 a diciembre de 2018 para tratar de encontrar publicaciones que, aun siendo menos actualizadas, pudieran aportar un conocimiento adicional. Así mismo, se consultaron revisiones sistemáticas y metaanálisis de los últimos 5 años para desarrollar los apartados de introducción y discusión del trabajo.
Para la estrategia de búsqueda se emplearon como palabras clave con el operador booleano “and”: melasma, treatment, topical treatment, hydroquinone, azelaic acid, kojic acid, arbutin, ascorbic acid, corticosteroids, retinoids, tranexamic acid, peeling, laser, ablative laser, non ablative laser, Q‑switched laser, picosecond laser, IPL, fractional radiofrequency, Platelet Rich Plasma, microneedling y sun protection.
Los criterios de inclusión fueron: idioma inglés, estudios con evidencia científica Ib (grado de recomendación A): clinical trial; realizados en hombres y mujeres de cualquier fototipo de piel; de edad igual o superior a 18 años. Se consideraron criterios de exclusión: idiomas diferentes al inglés, estudios con evidencia científica IIa/IIb, III y IV (grado de recomendación B/C); realizados en animales; edad inferior a 18 años o que incluyeran mujeres gestantes.
Inicialmente, se analizaron 166 abstracts en PubMed, descartándose 136 por ser artículos repetidos o tratar de lentiginosis, rejuvenecimiento, vitíligo o pacientes gestantes. Finalmente, se obtuvieron 30 abstracts que cumplían con los criterios establecidos y pasaron a la lectura completa, quedando incluidos un total de 19 ensayos clínicos y dos metaanálisis para el apartado discusión.
Resultados
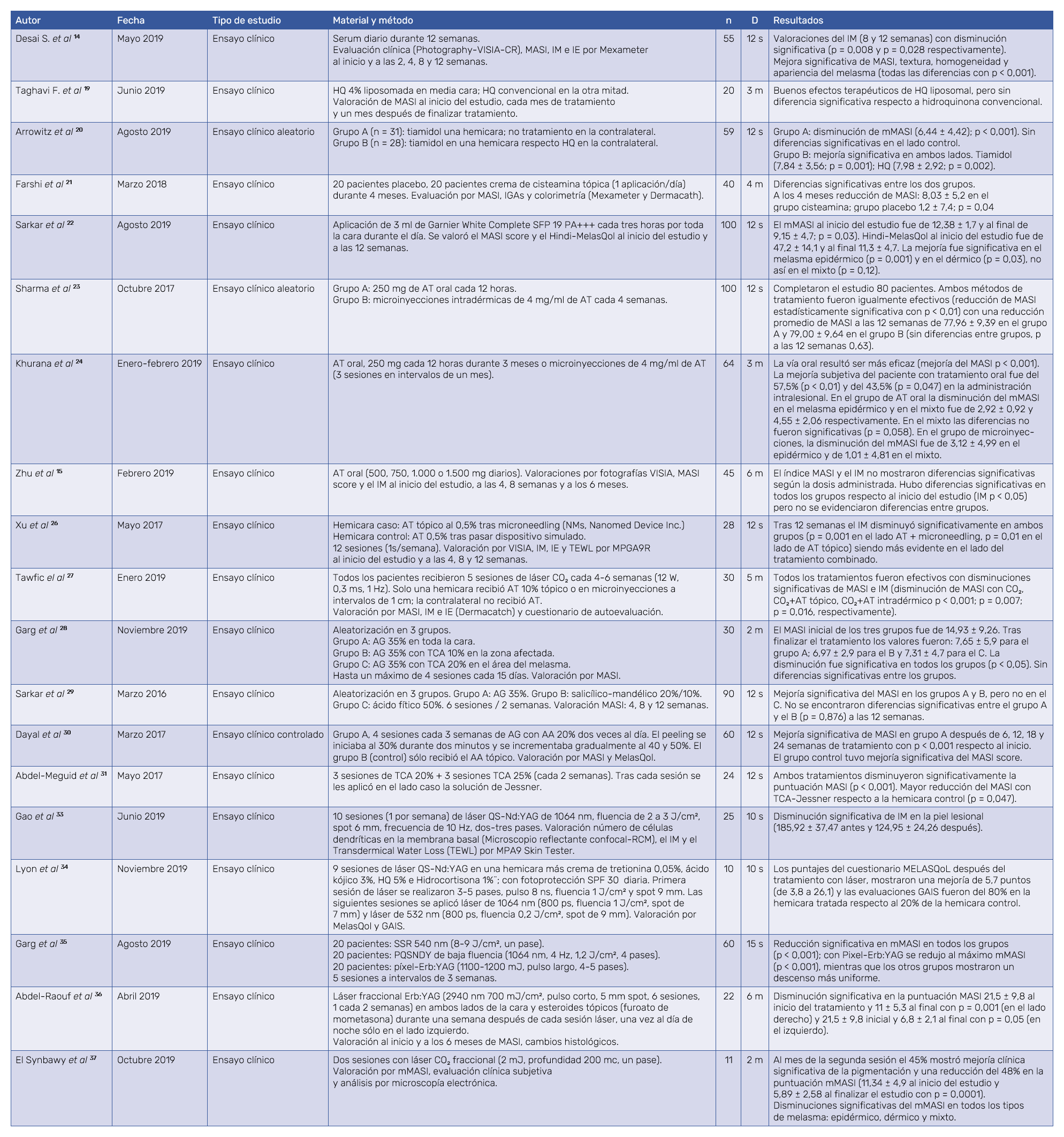
Los 19 ensayos clínicos que cumplían criterios quedan sistematizados en la Tabla I.
Discusión
La HQ tópica sigue siendo el tratamiento más estudiado, por su excelente perfil de seguridad y efectividad, en el tratamiento del melasma. El estudio de Taghavi et al19 mostró que la HQ en fórmula liposomal es igual de efectiva que la fórmula tradicional, aunque presenta menos efectos secundarios sobre la piel. La triple terapia combinada (TCC) continúa siendo el tratamiento más efectivo, aunque se han estudiado múltiples variaciones de su formulación original para disminuir los efectos adversos. Así, la combinación de ácido kójico, niacinamida y AT en serum ha demostrado mejorar la pigmentación en el melasma, pero no se ha comparado su efectividad respecto a la HQ o a la TCC14. En los últimos dos años se están investigando nuevos tratamientos tópicos para el melasma, como el tiamidol y la cisteamina20,21 El tiamidol ha demostrado tener una eficacia similar a la HQ mientras que la cisteamina, aunque es efectiva y mejora el aspecto del melasma epidérmico, no se ha comparado con HQ.
La fotoprotección es esencial para prevenir la exacerbación y recurrencias del melasma. No sólo la radiación ultravioleta A y B puede exacerbar el melasma, también la luz visible, en su espectro de radiación cercana (luz azul) puede empeorar el melasma. Por lo anterior, el uso de crema solar con FPS 50 o superior es obligatorio en el tratamiento del melasma, y debe contener filtros solares que protejan ante las radiaciones mencionadas y el infrarrojo cercano22.
El AT ha acaparado la atención en los últimos años, y cuenta con multitud de estudios para dilucidar la mejor vía de administración y las dosis óptimas de tratamiento. Se ha comparado la eficacia del AT en microinyecciones con la HQ tópica, encontrándose mejoría más rápida con el AT, a las 20 semanas no se encontraron diferencias significativas entre grupos23,24. Sin embargo, la vía de administración más utilizada es la oral, aunque no está libre de complicaciones y la dosis óptima diaria genera debate. Zhu et al han demostrado que no hay diferencias significativas en la dosis administrada (500, 1.000 o 1.500 mg/d)15, ni tampoco mayor riesgo de efectos trombóticos ni otras alteraciones de la coagulación; sólo efectos indeseables leves como dolor de cabeza, abdominal e hipomenorrea. No obstante, recomiendan realizar estudio de coagulación antes de iniciar tratamiento. Zhang et al indican que el AT es efectivo y seguro, y justifican su uso en el primer escalón terapéutico juntamente con los despigmentantes y la fotoprotección solar25. La dosis más recomendada de esta indicación off‑label sería de 250 mg 1 o 2 veces al día durante 3‑4 meses.
En orden a evitar complicaciones y mejorar la biodisponibilidad del AT se han empleado microinyecciones y microneedling23,24,26. Sharma et al23 compararon la administración oral de AT con las microinyecciones, evidenciando que ambas técnicas mejoraban significativamente el melasma pero sin diferencias entre grupos. En cambio Khurana et al24 encontraron mayor mejoría con AT oral (250 mg dos veces al día durante 3 meses) que con las microinyecciones (4 mg/ml). También, la administración tópica de AT también puede mejorar el aspecto del melasma con o sin microneedling previo26.
Otras estrategias para mejorar la liberación transdérmica de AT se basan en la apertura de microcanales mediante láser de CO₂ para facilitar la administración. Según el estudio de Tawfic et al27, las microinyecciones de AT tras el láser de CO₂ son más eficaces que administrar AT tópico. Sin embargo, los autores recomiendan no combinar las dos modalidades en una misma sesión para reducir la reacción inflamatoria y optimizar la efectividad del tratamiento.
En cualquier caso, el AT es un fármaco eficaz con un buen perfil de seguridad como indican los resultados del metaanálisis de Zang et al sobre la eficacia y seguridad del AT25. Incluyó 21 ensayos clínicos, realizados de 2006 a 2017, con 1563 pacientes. El análisis mostró beneficios en la administración oral, tópica e inyectable (tanto como tratamiento único como adyuvante) con mejorías del MASI. Se valoraron MASI, el índice de melanina (IM) e índice de eritema (IE) y se evidenciaron reducciones significativas del MASI score y del IM, pero no del IE. Los efectos secundarios fueron leves como reacciones gastrointestinales, oligomenorrea, hipopigmentación, urticaria y xerosis.
Los peelings superficiales con AG, AS y TCA deberían considerarse tratamientos de segunda línea. Los peelings con AG al 35% pueden ser útiles en el tratamiento del melasma28; Sarkar et al29 mostraron que los peelings de AG 35% y salicílico-mandélico 20% pueden mejorar el melasma en pieles oscuras, y Dayal et al30 alcanzaron resultados prometedores combinando AG (30‑50%) y AA. Las exfoliaciones con TCA combinadas con solución de Jessner podrían ser una alternativa prometedora en el tratamiento del melasma recalcitrante, pero se necesitan estudios de mayor tamaño muestral31. Inicialmente se podrían combinar con terapia tópica para los casos de melasma más graves, teniendo en cuenta el riesgo de eritema, ardor e HIP.
Los tratamientos láser han arrojado resultados heterogéneos, resultando difícil comparar resultados por la diversidad de dispositivos, fluencias y protocolos32. Hay coincidencia en no emplear el láser de Nd:YAG como tratamiento de primera línea por su alta tasa de recurrencias (40‑64%)33. Por el contrario, el láser de picosegundos induce un efecto fotomecánico destruyendo, supuestamente, los melanosomas pero manteniendo intacto el melanocito, lo que podría disminuir el riesgo de hipopigmentación34. Recientemente, se ha informado que el láser de Nd:YAG en modo Q‑switched a baja fluencia podría ser útil en el melasma epidérmico con menor riesgo de dolor y eritema35. El melasma dérmico o los casos recalcitrantes se pueden beneficiar con el láser de Er:YAG, con o sin combinación de esteroides tópicos36; mientras que el láser de CO₂ resulta útil en los 3 tipos de melasma: epidérmico, dérmico y mixto37. Tomados en conjunto los resultados, los láseres no pueden recomendarse de forma general para tratar el melasma, estando contraindicados aquellos que alcanzan altas fluencias32.
Tras cualquiera de los tratamientos empleados, solos o en combinación, la fotoprotección solar es obligada en el melasma17.
Conclusiones
El amplio abanico de opciones terapéuticas, así como la diversidad de estudios dificulta enormemente elegir un tratamiento óptimo. El tratamiento tópico con HQ sigue siendo la base del tratamiento del melasma. Los recientes estudios realizados demuestran la eficacia del AT así como su perfil de seguridad. La fotoprotección solar sigue siendo un pilar básico del tratamiento del melasma y, junto al AT y las sustancias despigmentantes tópicas, se ha de establecer como primer escalón terapéutico.
Los resultados suelen ser mejores cuando se hace una terapia combinada. No obstante, los tratamientos exfoliantes y el empleo de láseres deben estudiarse con grupos amplios de población en estudio metodológicamente bien diseñados para minimizar las numerosas variables que presentan.
Bibliografía
- Kutlubay Z, Cesur SK, Aşkın Ö, Tüzün Y. The color of skin: brown diseases of the skin, nails, and mucosa. Clin Dermatol. 2019 Sep‑Oct;37(5):487‑506. https://doi.org/10.1016/j.clindermatol.2019.07.007
- Alexis AF, Few J, Callender VD, Grimes P, Downie J, Boyd C, Gallagher CJ. Myths and Knowledge Gaps in the Aesthetic Treatment of Patients With Skin of Color. J Drugs Dermatol. 2019 Jul 1;18(7):616‑622.
- Ma Y, Millette D, Nalluri R, Yoo J. UK‑based dermatologist online survey on the current practice and training in the management of melasma and postinflammatory hyperpigmentation. Clin Exp Dermatol. 2020 Jun;45(4):483‑484. https://doi.org/10.1111/ced.14197
- Sarkar R, Jagadeesan S, Basavapura Madegowda S, Verma S, Hassan I, Bhat Y, Minni K, Jha A, Das A, Jain G, Arya L, Mandlewala Z, Bagadia J, Garg V. Clinical and epidemiologic features of melasma: a multicentric cross-sectional study from India. Int J Dermatol. 2019 Nov;58(11):1305‑1310. https://doi.org/10.1111/ijd.14541
- Kwon SH, Na JI, Choi JY, Park KC. Melasma: Updates and perspectives. Exp Dermatol. 2019 Jun;28(6):704‑708. https://doi.org/10.1111/exd.13844
- Rajanala S, Maymone MBC, Vashi NA. Melasma pathogenesis: a review of the latest research, pathological findings, and investigational therapies. Dermatol Online J. 2019 Oct 15;25(10):13030/qt47b7r28c. https://doi.org/10.5070/D32510045810
- Sarkar R, Bansal A, Ailawadi P. Future therapies in melasma: What lies ahead? Indian J Dermatol Venereol Leprol. 2020 Jan‑Feb;86(1):8‑17. Erratum in: Indian J Dermatol Venereol Leprol. 2020 Sep‑Oct;86(5):608. https://doi.org/10.4103/ijdvl.ijdvl_633_18
- Pereira AFC, Igarashi MH, Mercuri M, Pereira AF, Pinheiro ALTA, da Silva MS, Facchini G, Eberlin S. Whitening effects of cosmetic formulation in the vascular component of skin pigmentation. J Cosmet Dermatol. 2020 Jan;19(1):154‑160. https://doi.org/10.1111/jocd.12979
- Kumari S, Thng STG, Verma NK, Gautam HK. Melanogenesis inhibitors. Acta Dermato-Venereologica. Medical Journals 2018;98(10):924‑931. https://doi.org/10.2340/00015555-3002
- Janney MS, Subramaniyan R, Dabas R, Lal S, Das NM, Godara SK. A Randomized Controlled Study Comparing the Efficacy of Topical 5% Tranexamic Acid Solution versus 3% Hydroquinone Cream in Melasma. J Cutan Aesthet Surg. 2019 Jan‑Mar;12(1):63‑67.
- Rachmin I, Ostrowski SM, Weng QY, Fisher DE. Topical treatment strategies to manipulate human skin pigmentation. Adv Drug Deliv Rev. 2020 Jan 1;153:65‑71. https://doi.org/10.1016/j.addr.2020.02.002
- Pekmezci E. A novel triple combination in treatment of melasma: Significant outcome with far less actives. J Cosmet Dermatol. 2019 Dec;18(6):1700‑1704. https://doi.org/10.1111/jocd.12904
- Berardesca E, Rigoni C, Cantù A, Cameli N, Tedeschi A; Donne Dermatologhe Italia, Laureti T. Effectiveness of a new cosmetic treatment for melasma. J Cosmet Dermatol. 2020 Jul;19(7):1684‑1690. https://doi.org/10.1111/jocd.13203
- Desai S, Ayres E, Bak H, Manco M, Lynch S, Raab S, Du A, Green D, Skobowiat C, Wangari-Talbot J, Zheng Q. Effect of a Tranexamic Acid, Kojic Acid, and Niacinamide Containing Serum on Facial Dyschromia: A Clinical Evaluation. J Drugs Dermatol. 2019 May 1;18(5):454‑459.
- Zhu CY, Li Y, Sun QN, Takada A, Kawada A. Analysis of the effect of different doses of oral tranexamic acid on melasma: a multicentre prospective study. Eur J Dermatol. 2019 Feb 1;29(1):55‑58.
- Namazi N, Hesami A, Ketabi Y. The Split‑Face Comparison of the Combined Er‑YAG Laser and Hydroquinone 4% With Hydroquinone 4% Alone in the Treatment of Melasma in Iranian Patients: A Prospective, Interventional Case Study. J Lasers Med Sci. 2020 Winter;11(1):70‑73. https://doi.org/10.15171/jlms.2020.12
- Fatima S, Braunberger T, Mohammad TF, Kohli I, Hamzavi IH. The Role of Sunscreen in Melasma and Postinflammatory Hyperpigmentation. Indian J Dermatol. 2020 Jan‑Feb;65(1):5‑10. https://doi.org/10.4103/ijd.ijd_295_18
- Zubair R, Lyons AB, Vellaichamy G, Peacock A, Hamzavi I. What's New in Pigmentary Disorders. Dermatol Clin. 2019 Apr;37(2):175‑181. https://doi.org/10.1016/j.det.2018.12.008
- Taghavi F, Banihashemi M, Zabolinejad N, Salehi M, Jaafari MR, Marhamati H, Golnouri F, Dorri M. Comparison of therapeutic effects of conventional and liposomal form of 4% topical hydroquinone in patients with melasma. J Cosmet Dermatol. 2019 Jun;18(3):870‑873. https://doi.org/10.1111/jocd.12744
- Arrowitz C, Schoelermann AM, Mann T, Jiang LI, Weber T, Kolbe L. Effective Tyrosinase Inhibition by Thiamidol Results in Significant Improvement of Mild to Moderate Melasma. J Invest Dermatol. 2019 Aug;139(8):1691‑1698.e6. https://doi.org/10.1016/j.jid.2019.02.013
- Farshi S, Mansouri P, Kasraee B. Efficacy of cysteamine cream in the treatment of epidermal melasma, evaluating by Dermacatch as a new measurement method: a randomized double blind placebo controlled study. J Dermatolog Treat. 2018 Mar;29(2):182‑189. Erratum in: J Dermatolog Treat. 2020 Feb;31(1):104. https://doi.org/10.1080/09546634.2017.1351608
- Sarkar R, Ghunawat S, Narang I, Verma S, Garg VK, Dua R. Role of broad-spectrum sunscreen alone in the improvement of melasma area severity index (MASI) and Melasma Quality of Life Index in melasma. J Cosmet Dermatol. 2019 Aug;18(4):1066‑1073. https://doi.org/10.1111/jocd.12911
- Sharma R, Mahajan VK, Mehta KS, Chauhan PS, Rawat R, Shiny TN. Therapeutic efficacy and safety of oral tranexamic acid and that of tranexamic acid local infiltration with microinjections in patients with melasma: a comparative study. Clin Exp Dermatol. 2017 Oct;42(7):728‑734. https://doi.org/10.1111/ced.13164
- Khurana VK, Misri RR, Agarwal S, Thole AV, Kumar S, Anand T. A randomized, open‑label, comparative study of oral tranexamic acid and tranexamic acid microinjections in patients with melasma. Indian J Dermatol Venereol Leprol. 2019 Jan‑Feb;85(1):39‑43. https://doi.org/10.4103/ijdvl.ijdvl_801_16
- Zhang L, Tan WQ, Fang QQ, Zhao WY, Zhao QM, Gao J, Wang XW. Tranexamic Acid for Adults with Melasma: A Systematic Review and Meta-Analysis. Biomed Res Int. 2018 Nov 6;2018:1683414. https://doi.org/10.1155/2018/1683414
- Xu Y, Ma R, Juliandri J, Wang X, Xu B, Wang D, Lu Y, Zhou B, Luo D. Efficacy of functional microarray of microneedles combined with topical tranexamic acid for melasma: A randomized, self-controlled, split‑face study. Medicine (Baltimore). 2017 May;96(19):e6897. https://doi.org/10.1097/md.0000000000006897
- Tawfic SO, Abdel Halim DM, Albarbary A, Abdelhady M. Assessment of combined fractional CO2 and tranexamic acid in melasma treatment. Lasers Surg Med. 2019 Jan;51(1):27‑33. https://doi.org/10.1002/lsm.23032
- Garg S, Thami GP, Bhalla M, Kaur J, Kumar A. Comparative Efficacy of a 35% Glycolic Acid Peel Alone or in Combination With a 10% and 20% Trichloroacetic Acid Spot Peel for Melasma: A Randomized Control Trial. Dermatol Surg. 2019 Nov;45(11):1394‑1400. https://doi.org/10.1097/dss.0000000000001964
- Sarkar R, Garg V, Bansal S, Sethi S, Gupta C. Comparative Evaluation of Efficacy and Tolerability of Glycolic Acid, Salicylic Mandelic Acid, and Phytic Acid Combination Peels in Melasma. Dermatol Surg. 2016 Mar;42(3):384‑91. https://doi.org/10.1097/dss.0000000000000642
- Dayal S, Sahu P, Dua R. Combination of glycolic acid peel and topical 20% azelaic acid cream in melasma patients: efficacy and improvement in quality of life. J Cosmet Dermatol. 2017 Mar;16(1):35‑42. https://doi.org/10.1111/jocd.12260
- Abdel-Meguid AM, Taha EA, Ismail SA. Combined Jessner Solution and Trichloroacetic Acid Versus Trichloroacetic Acid Alone in the Treatment of Melasma in Dark-Skinned Patients. Dermatol Surg. 2017 May;43(5):651‑656. https://doi.org/10.1097/dss.0000000000001036
- Zhang Y, Zheng X, Chen Z, Lu L. Laser and laser compound therapy for melasma: a meta-analysis. J Dermatolog Treat. 2020 Feb;31(1):77‑83. https://doi.org/10.1080/09546634.2019.1577544
- Gao YL, Jia XX, Wang M, Hua Y, Zheng H, Xiang WZ, Song XZ. Melanocyte activation and skin barrier disruption induced in melasma patients after 1064 nm Nd:YAG laser treatment. Lasers Med Sci. 2019 Jun;34(4):767‑771. https://doi.org/10.1007/s10103-018-2658-7
- Lyons AB, Moy RL, Herrmann JL. A Randomized, Controlled, Split‑Face Study of the Efficacy of a Picosecond Laser in the Treatment of Melasma. J Drugs Dermatol. 2019 Nov 1;18(11):1104‑1107.
- Garg S, Vashisht KR, Makadia S. A prospective randomized comparative study on 60 Indian patients of melasma, comparing pixel Q‑switched NdYAG (1064 nm), super skin rejuvenation (540 nm) and ablative pixel erbium YAG (2940 nm) lasers, with a review of the literature. J Cosmet Laser Ther. 2019 Aug;21(5):297‑307. https://doi.org/10.1080/14764172.2019.1605447
- Abdel-Raouf Mohamed H, Ali Nasif G, Saad Abdel-Azim E, Abd El‑Fatah Ahmed M. Comparative study of fractional Erbium: YAG laser vs combined therapy with topical steroid as an adjuvant treatment in melasma. J Cosmet Dermatol. 2019 Apr;18(2):517‑523. https://doi.org/10.1111/jocd.12751
- El‑Sinbawy ZG, Abdelnabi NM, Sarhan NE, Elgarhy LH. Clinical & ultrastructural evaluation of the effect of fractional CO2 laser on facial melasma. Ultrastruct Pathol. 2019;43(4‑5):135‑144. https://doi.org/10.1080/01913123.2019.1673861


